臨床研究センター
更新日:<お問い合わせ先>臨床研究推進室
- TEL:
- 072-272-1199(代表)
- メール:
- chikenkanri★sakai-hospital.jp
(治験関連)
kenkyu★sakai-hospital.jp
(臨床研究関連)
- ★は@に書き換えてください
お知らせ
- {{item.date}}
- {{item.title}}
センター長の挨拶
2023年4月から臨床研究センター長を拝命いたしました能浦真吾です。
臨床研究とは、人を対象として行われる医学研究のことで、新しい薬や手術、放射線治療などを用いた新しい治療、あるいはそれらの組み合わせで行われる治療法などに対して、その効果や安全性について確認するために行われる試験のことを臨床試験といいます。
当センターでは、この倫理指針を遵守したうえで臨床研究が積極的に実施されるように支援を行っております。今後ともみなさんのご理解とご協力をお願い申し上げます。
臨床研究センター長
能浦 真吾
臨床研究センターの紹介・組織図
臨床研究センターは、当院における治験及び臨床研究を推進し、当院職員が治験及び臨床研究を円滑かつ適切に実施できるよう支援しています。また、被験者の皆様の人権や安全を守り、適正な治験、臨床研究が実施されるよう支援しています。
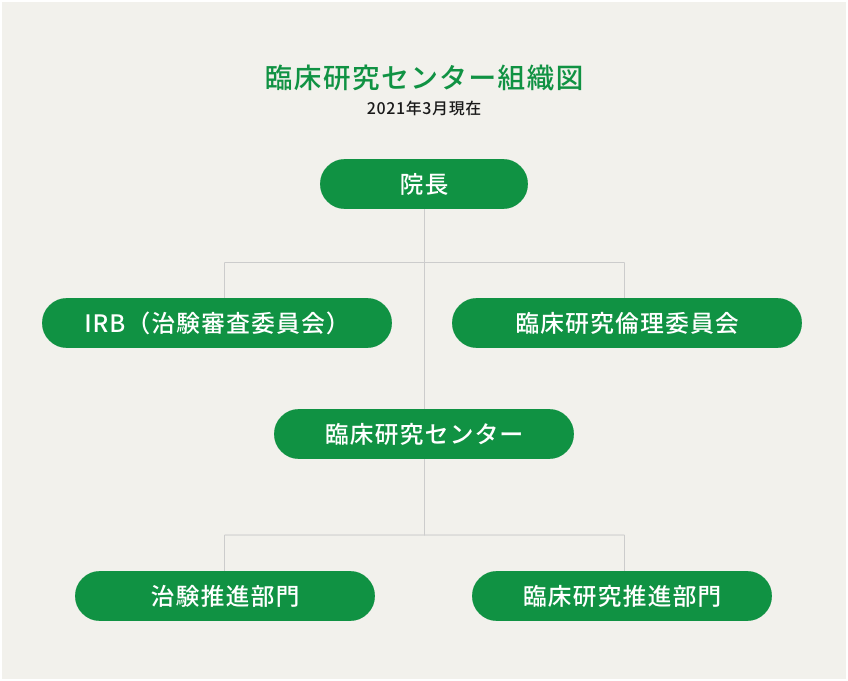
センターの主な業務内容
- 治験及び臨床研究の実施体制整備
- 治験及び臨床研究の教育啓発活動
- 治験及び治験審査委員会に関する支援業務
- 臨床研究及び臨床研究倫理委員会に関する支援業務
センター員の構成
- 医師 5名
- 看護師 1名
- 薬剤師 1名
- 臨床検査技師 1名
- CRC 1名(看護師)
- 事務 1名
スタッフ紹介
能浦 真吾のうら しんご消化器外科 部長
大腸肛門外科 医員
臨床研究センター センター長
- 大学
- 大阪大学(平成5年)
- 専門分野
- 大腸外科
消化器外科
- 認定資格
- 医学博士(大阪大学)
日本外科学会 認定医・専門医・指導医
日本消化器外科学会 専門医・指導医
日本大腸肛門病学会 専門医・指導医
日本内視鏡外科学会 技術認定医(大腸)
ロボット(da Vinci)手術 認定医
日本ロボット外科学会 専門医
日本消化器病学会 専門医・指導医
日本ストーマ・リハビリテーション学会 ストーマ認定士
日本消化器病学会 専門医・指導医
- 学会
- 日本外科学会
日本消化器外科学会
大腸癌研究会(世話人)
日本大腸肛門病学会(評議員)
日本内視鏡外科学会(評議員)
日本臨床外科学会(評議員)
日本外科系連合科学会(評議員)
日本外科感染症学会(評議員)
日本ストーマ・リハビリテーション学会(評議員)
日本ロボット外科学会
日本消化器病学会
日本癌治療学会
日本消化管学会
日本腹部救急医学会
日本遺伝性腫瘍学会

ニュースレター
セミナー開催履歴
当センターでは、院内の研究者に対し、臨床研究セミナーを実施しています。臨床研究センターのスタッフが中心となって企画・運営を行っています。
←表を左右にスクロールできます→
| 開催年度 | タイトル |
|---|---|
| 2023年度 | 臨床研究実施におけるポイント |
| 2022年度 | サクッと統計解析 ~ EZR の使い方 ~ |
| 2022年度 | 臨床研究における文書同意について |
| 2021年度 | 学会発表における倫理審査 |
| 2021年度 |
|
| 2020年度 | ~臨床研究を始めたい人へ~ |
| 2019年度 | 臨床研究における『被験者保護』を考えよう ~被験者保護ってなぁに?~ |
| 2019年度 | 医薬品医療機器総合機構(PMDA)のGCP実地調査を経験して |
| 2018年度 | 第1部:~治験ってなあに?~ 第2部:治験を実施する医療機関に求められること |
| 2018年度 | 臨床研究法新時代到来 ~いつまでに何をすればいいの?~ |
治験の品質向上への取り組み
学会発表
2022年度
←表を左右にスクロールできます→
| 開催日 | 学会等 | 演題 |
|---|---|---|
| 9月17日~9月18日 | 第22回 CRCと臨床試験のあり方を考える会議2022in新潟(ポスター発表) 「優秀演題賞」を受賞! |
「治験業務マニュアル」を用いた品質管理向上作戦 :SMOのCRCと共同で取り組んだ継続的な治験業務活動 |
2020年度
←表を左右にスクロールできます→
| 開催日 | 学会等 | 演題 |
|---|---|---|
| 11月3日~11月16日 (WEB開催) |
第20回 CRCと臨床試験のあり方を考える会議2020 in 長崎(ポスター発表) | 堺市立総合医療センターにおける治験の品質管理向上を目指した取り組み~「治験業務マニュアル」作成・運用の試み~ |
